Schädigt die Behandlung von Augenkrankheiten mittels RNA-Interferenz den Sehsinn ?
Nackte, extrazellulär verabreichte siRNAs seien für die Behandlung von Augenkrankheiten nicht geeignet: sie könnten ein Spätstadium der trockenen Makuladegeneration verursachen. Dies behauptet eine vor Kurzem im New England Journal of Medicine veröffentlichte Studie.
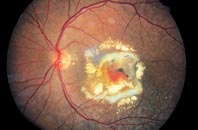
(9. September 2008) Im späten Stadium der trockenen Form der Makuladegeneration kommt es zur geographischer Atrophie: Zellverbände im retinalen Pigmentepithel sterben flächenhaft ab. Daraufhin degenerieren die über diesen Läsionen liegenden Photorezeptoren der Makula und die darunter liegenden Kapillaren der Aderhaut. Das scharfe Sehen im Zentrum des Gesichtsfeldes verschlechtert sich.
Eine Ende August im
New England Journal of Medicine veröffentliche Studie von Yang
et al. (
N Engl J Med 2008; 359 ) an Amerikanern europäischer Abstammung ergab, dass eine Toll-like Receptor 3 (TLR3)-Variante mit der Aminosäure Phenylalanin an Position 412 (412F) vor geographischer Atrophie schützt. Die 412F Variante des TRL3 soll das Erkrankungsrisiko um 30 bis 70 Prozent senken, die TLR3-Form mit Leucin an Position 412 (412L) dagegen nicht. Das Allel für die 412F Variante ist bei Asiaten und Amerikanern europäischer Abstammung häufig, bei Afrikanern dagegen selten.
Yang
et al. fanden zudem Hinweise, dass extrazellulär verabreichte, nackte siRNAs zur Behandlung der Makuladegeneration ungeeignet sind. Nackte siRNAs können zwar die Gefäßneubildung in der Aderhaut des Auges hemmen (siehe http://www.laborjournal.de/rubric/archiv/editorials/302.html), induzieren aber auch den Tod anderer Zelltypen und führen so zu einer weiteren Schädigung des Sehsinns. So binden lange doppelsträngige RNAs wie poly(I:C) an den TLR3 und aktivieren ihn. Dies kann Apoptose und den Tod der Zelle auslösen und stellt einen Schutz vor Virusinfektionen dar. Für den TLR3-Mechanismus spricht folgender Befund von Yang
et al.: Die Injektion von langer, doppelsträngiger poly(I:C) RNA in den Glaskörper des Auges löst bei Wildtyp-Mäusen geographische Atrophie aus, mit deutlich erhöhten Zelltod- und Apoptoseraten von Pigmentepithelzellen der Retina, bei TLR3 Knock Out-Mäusen treten jedoch keine Symptome auf.
Da lange doppelsträngige RNAs bei Virusinfektionen gebildet werden, spielen also vielleicht virale Augeninfektionen und virale doppelsträngige RNA bei der Entstehung der geographischen Atrophie eine Rolle.
Yangs Ergebnisse zeigen auch, dass extrazellulär verabreichte nackte siRNAs zur Behandlung von Augenkrankheiten ungeeignet sind: siRNAs können geographische Atrophie verursachen. Dies hängt allerdings vom TLR3-Rezeptortyp ab, denn die 412 F Variante TLR3 schützt vor der cytotoxischen Wirkung nackter siRNAs (siehe oben). Auch zeigten Primäre menschliche Retina-Pigmentepithelzellen mit zwei Allelen für die TLR3-Form 412L
in vitro doppelt so hohe Zelltod- und Apoptoseraten wie Zellen mit je einem Allel für 412F und 412L. Die TLR3-Variante 412F ist im Vergleich zur 412L-Form weniger präsent auf der Zelloberfläche und schwerer aktivierbar durch doppelsträngige RNA.
Eine in
nature (
452: 591-597, 2008 ) veröffentlichte Vorgängerstudie unter der Leitung von Jayakrishna Ambati von der Universität Kentucky ergab, dass die Rezeptorvariante 412F auch Endothelzellen der Aderhaut des Auges vor den cytotoxischen Effekten extrazellulär verabreichter siRNAs schützt. Ambati will nun in klinischen Studien TLR3-Inhibitoren zur Vorbeugung der geographischen Atrophie testen.
Die Firmen
Allergan und
Opko Health führen mit den siRNA-Medikamenten
siRNA-027 und
bevasiranib zur Therapie der feuchten Form der Makuladegeneration derzeit klinische Phase II und III-Studien an Patienten durch. In diesen soll auch die Sicherheit und Wirksamkeit der Medikamente untersucht werden. Sam Reich, ein Vertreter von
Opko Health, hält die Studie von Yang
et al. für wenig gewichtig. Eine Fülle von Publikationen würden die spezifische Wirksamkeit von siRNAs bestätigen. Bei 200 Patienten, an welchen die Firma
bevasiranib getestet habe, habe es über einen Zeitraum von zwei Jahren und länger keine bedeutenden Nebenwirkungen gegeben.
Man darf gespannt sein, wie dieser Widerspruch aufgelöst werden wird. Falls Yang
et al. doch recht haben, könnte die Abschirmung der siRNAs durch chemische Modifikation oder Verpackung in Lipidkügelchen das Problem lösen.
Bettina Dupont Quellen: innovations report, nature
Letzte Änderungen: 09.09.2008





 (9. September 2008) Im späten Stadium der trockenen Form der Makuladegeneration kommt es zur geographischer Atrophie: Zellverbände im retinalen Pigmentepithel sterben flächenhaft ab. Daraufhin degenerieren die über diesen Läsionen liegenden Photorezeptoren der Makula und die darunter liegenden Kapillaren der Aderhaut. Das scharfe Sehen im Zentrum des Gesichtsfeldes verschlechtert sich.
(9. September 2008) Im späten Stadium der trockenen Form der Makuladegeneration kommt es zur geographischer Atrophie: Zellverbände im retinalen Pigmentepithel sterben flächenhaft ab. Daraufhin degenerieren die über diesen Läsionen liegenden Photorezeptoren der Makula und die darunter liegenden Kapillaren der Aderhaut. Das scharfe Sehen im Zentrum des Gesichtsfeldes verschlechtert sich.