Tipp 47:
Thermoblöcke selbst gebastelt
Kühles für einen heißen Sommer
Biologische Proben müssen eiskalt bleiben, sonst gibt's einen Satz heißer Ohren vom Chef. Wie das geht, wenn das Thermometer immer höher klettert, lesen Sie hier.
Der Sommer lockt mit Baggerseetemperaturen, und des fleißigen Wissenschaftlers Gedanken wandeln auf den Spuren des schwedischen Astronomieprofessors Anders Celsius, der 1742 die hundertteilige Temperaturskala – ausgehend vom Eis- und Siedepunkt des Wassers – vorschlug. LJ-Autor Ralph Schill aus Tübingen jedoch stellte sich nicht die Frage, ob es ihm selbst zu warm sei, sondern vielmehr, wie viel Grad Celsius das Probenmaterial erträgt, bevor Artefakte den Spaß an der Forschung vermiesen.
"Um genau diese zu verhindern, wurden vollelektronisch-regulierte Kühlblöcke erfunden. Einfach die gewünschte Temperatur über dem Display eingeben, und die Cups werden auf die Wohlfühltemperatur der jeweiligen Proben gebracht und gehalten. Diese liegt meist irgendwo zwischen 0 °C und 4 °C, damit auch normales Eis aus der Eismaschine oder dem Tiefkühlschrank eine Chance auf Verwendung hat. Eine Schaufel "crushed Ice" in eine Styroporbox, und schon können die Cups, eins nach dem anderen, in eine kühle Position gebracht werden. Die Praxis zeigt allerdings, dass die Berge und Täler des Eises immer wieder mal Cups zum kippen bringen und im schlechtesten Fall hat man dann das Tagewerk durch Eiskrümel kontaminiert. Eine saubere Lösung sind die bereits erwähnten Thermo- oder gekühlte Metallblöcke. Erstere sind jedoch sehr teuer und die Metallblöcke, na ja, meist war ein Kollege schneller und hat sich den letzten geschnappt. Bleibt nur, sich Blöcke selbst zu basteln und das maßgeschneidert für die jeweilige Anwendung.
Die Lösung: Selber Basteln
Hierzu klebt man einfach Cups mit dem geschlossenen Deckel auf eine Kunststoffplatte (Bild 1), die dann in eine Schüssel mit entmineralisierten oder destillierten Wasser gehängt und über Nacht in die Tiefkühltruhe gestellt wird. Am nächsten Morgen mit ein wenig schütteln die Platte mit den Cups aus der Schüssel geklopft und fertig ist der passgenaue Abguss (Bild 2). Der Eisblock kann in der Schüssel verbleiben oder man legt ihn in eine flache Styroporkiste. Die Cups mit dem Probenmaterial stehen standsicher in der Form und werden entsprechend gut gekühlt. So ein Block hält nach eigenen Erfahrungen nahezu einen ganzen Arbeitstag und kann nach Benutzung im Waschbecken zum Schmelzen freigegeben werden. Eine Kontamination von Vorbenutzern ist mit dieser Einweglösung nahezu ausgeschlossen und man kann die Blöcke gut auf Vorrat fertigen und im Tiefkühlschrank lagern.
Bleibt die Frage: Wie gefriere ich Gewebeproben, Proteine oder RNA möglichst schnell am Arbeitsplatz weg, ohne das Dewargefäß neben sich stehen zu haben und ständig vom Stickstoff umnebelt zu sein? Ganz nebenbei kommen bei flüssigem Stickstoff mit seinen196 °C gerne als Isolationseffekte bezeichnete Phänomene vor: Da die Siedetemperatur von flüssigem Stickstoff mit -183 °C sehr nahe der Verflüssigungstemperatur ist, kann ein eingetauchtes, warmes Objekt den Stickstoff zum Kochen bringen. Der flüssige Stickstoff geht dabei in die Gasphase über und kann eine dünne Isolationsschicht um das Cup bilden welches die kryogene Wirksamkeit herabsetzt. Wer eine konstante Gefriertemperatur haben möchte, verwendet Isopentan (2-Methylbutan).
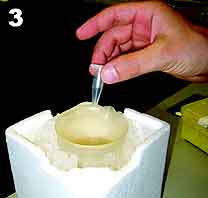
Mit flüssigem Stickstoff gekühltes Isopentan wird ab -160 °C immer visköser und garantiert eine konstante Temperatur, direkt am Cup anliegend. Auch in Kombination mit Trockeneis (-78 °C) ist Isopentan oder Ethanol sehr nützlich. Trockeneis selbst ist ein Kontaktkryogen, welches kein homogenes Gefrieren ermöglicht und daher vermieden werden sollte. Stellt man aber einen Becher mit einem dieser Alkohole in eine Box voll Trockeneis (Bild 3), so hat man eine ebenso geeignete Kälteleitung wie direkt in der -80° Truhe – und muss nicht in einer Stickstoff- oder Kohlendioxidwolke arbeiten."
Letzte Änderungen: 08.09.2004